ハイポキシア細胞特異的核酸医薬創製を指向したペプチドリボ核酸 (PRNA)
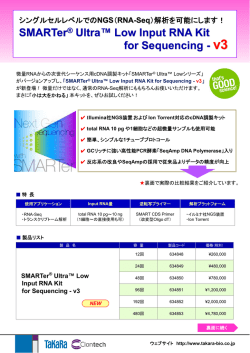
第 25 回仙台シンポジウム Poster 発表要旨 ハイポキシア細胞特異的核酸医薬創製を指向したペプチドリボ核酸 (PRNA)の開発 Development of Peptide Ribonucleic Acid (PRNA) Aiming for Hypoxia Specific Oligonucleotide Therapeutics 上松亮平、荒木保幸、坂本清志、和田健彦(東北大学多元物質科学研究所) ハイポキシアは、低酸素症とも呼ばれ、細胞が正常に機能するために必要な酸素の供給が不足してい る状態である。酸素不足で引き起こされる解糖系の亢進により、細胞内に乳酸が蓄積し、細胞内 pH が低 下する。ハイポキシアの原因として、脳梗塞、心筋梗塞による酸素供給の遮断や、増殖期がん細胞内での 血管新生遅滞による酸素供給力の低下が挙げられる。 我々は細胞内 pH 応答性人工核酸としてペプチドリボ核酸(PRNA)を開発し、その特性について報告し てきた 1)。PRNA は、ハイポキシア状態の細胞特有の酸性条件下においては塩基部が anti 配向を優先し、 標的 RNA と錯体を形成し効果的な核酸医薬として機能する。それに対し、中性条件下では、分子内に導 入したボロン酸ユニットとリボース環-ボロン酸のボロン酸エステルを形成し、これによって塩基部の syn 配向 への変化が誘起される。この配向変化により、PRNA は標的 RNA の認識・結合能を喪失し、薬効を失う。 即ち、PRNA はハイポキシア細胞内特異的に薬効を発現する核酸医薬としての応用が期待される(図 1)。 しかしながら、ハイポキシアの細胞は、その病態や細胞種により pH が異なることが知られており 2)、標的 細胞に応じた pH で薬効を発現するように PRNA のボロン酸エステル形成を制御する必要がある。 このような背景を踏まえ、置換基の導入による動作 pH 制御に取り組んだ。まず、種々の置換基を有する フェニルボロン酸との分子間結合を滴定実験により検討した。さらに、フェニルボロン酸を内部因子化した PRNA を合成し、同様の滴定実験により、分子内結合の検討を行った。分子間反応、分子内反応ともにボ ロン酸エステル形成反応を起こすスイッチング pH 帯が Hammett 則に従うことが明らかとなった。興味深い Switch on Switch off ことに、分子内反応では、分子 間反応と比較してスイッチング H target RNA PRNA PRNA HN H target RNA O H N N HN H O H N N O O O O N OH N N H N OH N pH 帯の変化と、結合定数の大 N NH NH O O N N NH HN O N N O O O O O O O HO 幅な増大がみられた。 OH O B O OH OH O O B O O P OH HN P O O 本発表では、この置換基効 O O HN O O 果による PRNA の作動 pH の制 (pH 7.2) 御について、CD および NMR 図 1. ハイポキシア特異的核酸医薬 スペクトルにより詳細に検討し た結果を報告する。 <参考文献> 1)(a) Wada, T.; Minamimoto, N.; Inaki, Y.; Inoue, Y., J. Am. Chem. Soc. 2000, 122 (29), 6900-6910; (b) 和田健彦, 刺激応答性人工核酸, 核酸化学のニュートレンド‐DNA・RNA の新たな可能性を拓く‐, 化学同人, 71-77 (2011). 2)(a) Wike-Hooley, J. L.; Haveman, J.; Reinhold, H. S., Radiother. Oncol. 1984, 2 (4), 343-366. (b) Petroff, O. A. C.; Prichard, J. W.; Behar, K. L.; Alger, J. R.; den Hollander, J. A.; Shulman, R. G., Neurology, 1985, 35 (6), 781. (c) Vaupel, P.; Kallinowski, F.; Okunieff, P., Cancer Res., 1989, 49 (23), 6449-6465. 発表者紹介 氏名 上松 亮平 (うえまつ りょうへい) 所属 東北大学多元物質科学研究所 東北大学大学院理学研究科化学専攻 学年 博士課程後期 2 年 研究室 生命機能制御物質化学研究分野(和田研究室)
© Copyright 2026